Saúde
A Canábis na Epilepsia
Publicado
3 anos atrásem
Por
Soraia Tomás
Definida pela Organização Mundial de Saúde (OMS) como um «transtorno neurológico crónico que atinge pessoas de todas as idades», a Epilepsia afecta mais de 50 milhões de pessoas em todo o mundo. Em Portugal, estima-se que existam cerca de 50 mil pessoas com esta doença. O papel que o sistema endocanabinóide desempenha na génese da Epilepsia providencia a base farmacológica que deve fomentar a investigação do uso de canabinóides exógenos, como os fitocanabinóides produzidos pela canábis no tratamento da Epilepsia.
A Epilepsia é uma perturbação do sistema nervoso caracterizada por uma predisposição duradoura para gerar crises epilépticas e pelas consequências neurobiológicas, cognitivas, psicológicas e sociais das mesmas.
Nos últimos anos, o CBD (canabidiol) tem-se revelado como uma arma terapêutica extremamente relevante. As suas propriedades anti-convulsivantes, aliadas à reduzida toxicidade para o organismo, tornaram este canabinóide numa ferramenta valiosa no controlo de crises epilépticas refractárias a outros medicamentos.
Vários estudos comprovam também as propriedades neuro-protectoras do CBD, que reduzem a hiperexcitabilidade neuronal e preservam, desta forma, as capacidades cognitivas, reduzindo a progressão dos danos causados no sistema nervoso devido a convulsões repetidas.
Crises Epilépticas e Epilepsia
Uma crise epiléptica é a ocorrência transitória de sinais e/ou sintomas devidos a uma actividade neuronal excessiva ou síncrona no cérebro, com duração variável (geralmente entre alguns segundos a vários minutos); i.e., é um evento resultante de uma disfunção temporária da actividade eléctrica cerebral.
A Epilepsia, por sua vez, é uma doença que se expressa através de crises epilépticas recorrentes (duas ou mais, separadas por intervalos superiores a 24 horas, ou uma crise única associada a um elevado risco avaliado de repetição), súbitas e imprevisíveis, incontroláveis pelo doente (i.e., não provocadas ou reflexas).
Fala-se em Epilepsia quando ocorrem, pelo menos, dois episódios de convulsões não relacionados com a abstinência alcoólica, hipoglicémia, problemas cardíacos ou outros. Em alguns casos, basta uma convulsão para se fazer o diagnóstico da Epilepsia, desde que exista um risco elevado de ocorrência de mais.
Causas
As possíveis causas de Epilepsia são:
- Genéticas: quando a Epilepsia é entendida como o resultado directo de um defeito genético conhecido ou presumido e em que as crises são o principal sintoma da doença (por exemplo, mutações no gene SCN1A e síndrome de Dravet). Não exclui a possibilidade de que factores do meio ambiente (fora do indivíduo) possam contribuir para a expressão da doença.
- ”Estruturais/metabólicas”: quando existe uma condição distinta estrutural ou metabólica ou outra doença que demonstrou estar associada a um substancial aumento do risco de desenvolver Epilepsia. Lesões estruturais incluem distúrbios adquiridos como acidente vascular cerebral, trauma e infecção. Algumas das causas estruturais são de origem genética (por exemplo, esclerose tuberosa ou algumas malformações do desenvolvimento cortical).
- ‘‘Causa desconhecida’‘: é uma forma neutra para designar que a natureza da causa subjacente não é, ainda, conhecida; pode haver um defeito genético fundamental ou pode ser a consequência de um distúrbio separado ainda não reconhecido. Esta causa representa uma percentagem muito significativa dos casos.
Tipos de crises
As crises não se manifestam todas de forma igual e a mesma pessoa pode apresentar crises distintas.
Crise epiléptica parcial – A descarga eléctrica tem lugar numa zona reduzida da superfície cerebral. Por vezes, generaliza-se e atinge o resto do cérebro. Os sintomas diferem consoante a zona do cérebro onde ocorre a descarga. Na zona motora cerebral manifesta-se através de movimentos involuntários de um lado do corpo, sem perda de consciência. Na região da sensibilidade pode provocar uma alteração sensitiva focal transitória como, por exemplo, um formigueiro. Na zona visual pode provocar uma visão de luzes.
Crise epiléptica generalizada – A descarga eléctrica afeta toda a superfície cerebral ao mesmo tempo.
Crise generalizada tónico-clónica – Está associada a perda de consciência. A pessoa cai imediatamente no chão. Manifesta-se também através de movimentos involuntários dos membros. Morder a língua, espumar pela boca e incontinência urinária são outras das manifestações deste tipo de crise.
Crise generalizada de ausência – A pessoa fica imóvel, desligada do meio envolvente, com o olhar fixo, durante 10 a 15 segundos. Este tipo de crise é comum em crianças e adolescentes. E tende a desaparecer com a idade. Pode provocar quebras no rendimento escolar por défices de atenção e de aprendizagem.
Crise mioclónica – Caracteriza-se por tremores súbitos de todo ou parte do corpo durante alguns segundos.
Crise generalizada atónica – Implica uma perda brusca do tónus muscular e da consciência, que dura apenas alguns segundos e da qual se recupera em poucos segundos também.
Sintomas
Existem vários tipos de crises epilépticas. Dependendo do tipo de crises, pode haver um ou mais dos seguintes sinais:
- Olhar fixo (5-10 segundos), sem resposta à estimulação;
- Perda súbita da força muscular com queda;
- Pestanejo rápido ou revulsão ocular;
- Movimentos da boca (mastigação) ou da face;
- Movimentos rítmicos (“estrebuchar”) de todo ou parte do corpo;
- Rigidez muscular (hipertonia)
- Perda de urina / fezes;
- Mordedura da língua / bochecha;
- Perda de consciência com queda;
- Comportamento confuso, sem objectivo;
- Relato de sensações subjectivas (sensitivas, sensoriais, cognitivas ou emocionais)
Tratamento
O tratamento deve ser altamente personalizado, devendo tomar em consideração os seus próprios riscos e os perigos de mais crises convulsivas. É, por isso, importante ponderar a idade do paciente, as características dos ataques, os factores associados e o contexto social e profissional. Muitos dos medicamentos anti-epilépticos apresentam efeitos secundários relevantes e esse risco requer uma adequada ponderação.
O Sistema Endocanabinóide e a Epilepsia
O Sistema Endocanabinóide (SEC) é um sistema endógeno (que tem origem no interior), presente em todos os seres vertebrados, e está associado a vários processos fisiológicos como a regulação neuronal, regulação do apetite, energia, imunidade [1] e reprodução [2].
Este sistema envolve receptores canabinóides, endocanabinóides e enzimas, que sintetizam e metabolizam endocanabinóides.  Os endocanabinóides são lípidos mediadores, derivados de cadeias de ácidos gordos polinsaturados que têm a capacidade de modular vários processos incluindo a reprodução de mamíferos [3]. São sintetizados “on demand’” a partir de percursores fosfolipídicos que se localizam na membrana plasmática das células [4]. Este metabolismo resulta na produção de dois canabinóides endógenos, a anandamida (AEA) e o 2-araquidonoilglicerol (2-AG). O primeiro alvo da AEA e 2-AG são os receptores canabinóides (CB1 e CB2) [1] expressos nos tecidos periféricos, aos quais se acoplam, activando mecanismos de sinalização intracelular. Além destes últimos, a AEA e o 2-AG têm também afinidade para os receptores GPR55, GPR119, receptor activado por proliferadores de perixoma (PPAR) e receptor de potencial transiente vanilóide 1 (TRPV1).
Os endocanabinóides são lípidos mediadores, derivados de cadeias de ácidos gordos polinsaturados que têm a capacidade de modular vários processos incluindo a reprodução de mamíferos [3]. São sintetizados “on demand’” a partir de percursores fosfolipídicos que se localizam na membrana plasmática das células [4]. Este metabolismo resulta na produção de dois canabinóides endógenos, a anandamida (AEA) e o 2-araquidonoilglicerol (2-AG). O primeiro alvo da AEA e 2-AG são os receptores canabinóides (CB1 e CB2) [1] expressos nos tecidos periféricos, aos quais se acoplam, activando mecanismos de sinalização intracelular. Além destes últimos, a AEA e o 2-AG têm também afinidade para os receptores GPR55, GPR119, receptor activado por proliferadores de perixoma (PPAR) e receptor de potencial transiente vanilóide 1 (TRPV1).
Ao produzirem o efeito pretendido, os endocanabinóides AEA e 2-AG são degradados por enzimas especificas que incluem a hidrolase da amida de ácidos gordos (FAAH) e a lípase de monoacilglicerol (MAGL), respectivamente, ou por endocitose.
Actualmente, sabe-se que tanto os endocanabinóides como os fitocanabinóides actuam nas extremidades dos neurónios, afectando a neurotransmissão pela sua ação a nível dos receptores canabinóides, com elevados níveis de receptores localizados na membrana pré-sináptica e os componentes de síntese de endocanabinóides encontrados na membrana pós-sináptica. No entanto, os endocanabinóides também actuam noutras células do Sistema Nervoso Central (SNC), tais como as células gliais (astrócitos e microglia) e são produzidos por diversos neurónios e células (ex. oligodendrócitos). Os canabinóides afectam a vasculatura do SNC. [5][6][7]
O receptor CB1 está acoplado à proteína G e é expresso na membrana pré-sináptica dos terminais axonais. Quando a membrana pré-sináptica sofre despolarização, a AEA e o 2-AG são sintetizados na membrana pós-sináptica e libertadas na fenda sináptica, acoplando-se aos receptores CB1 localizados na pré-sináptica. Ao activarem estes receptores, causam hiperpolarização transitória da membrana pré sináptica, suprimindo os canais de voltagem de cálcio e ativando os de K+. Esta hiperpolarização transitória dos canais pré-sinápticos inibe a libertação de certos neurotransmissores. [8] Durante uma crise epiléptica, a libertação excessiva de neurotransmissores excitatórios, como o glutamato, resulta na activação de receptores CB1 na membrana pré-sináptica. Este mecanismo de feedback negativo, produzido pelos receptores CB1, resulta na diminuição da libertação de glutamato, desempenhando assim um papel fundamental no controlo da hiperexcitabilidade neuronal, prevenindo as convulsões.
Ao examinarem o tecido cerebral, removido cirurgicamente de um paciente com epilepsia, cientistas observaram uma baixa expressão de receptores CB1 nos terminais axonais de neurónios glutaminérgicos, o que resulta numa inibição anormal do controlo da libertação de glutamato. Relataram ainda elevados níveis de receptores CB1 terminais axonais de neurónios gabaminérgicos, inibindo desta forma a libertação de GABA (ácido gama-aminobutírico). [9] O conjunto destes dois factores resulta num estado de hiperexcitabilidade neuronal, que aumenta a probabilidade de ocorrência de convulsões. [10]
O papel que o sistema endocanabinóide desempenha na génese da Epilepsia providencia a base farmacológica que deve fomentar a investigação do uso de canabinóides exógenos, como os fitocanabinóides produzidos pela planta canábis no tratamento da epilepsia.
Canábis e Epilepsia
O potencial terapêutico da canábis na Epilepsia e convulsões está documentado ao longo da História. A planta canábis contém mais de 160 canabinóides que, individualmente e colectivamente, actuam de diversas formas no Sistema Nervoso Central (SNC) dos mamíferos. [11]
O canabinol (CBN) e o canabidiol (CBD) foram isolados pela primeira vez em 1940 e o D9-tetrahidrocanabinol (THC) em 1942 [12][13]. A estrutura química do CBD foi caracterizada por Mechoulam e Shvo em 1963 e de seguida a elucidação da estrutura do THC em 1964. [14][15] O THC foi o primeiro fitocanabinóide a ser analisado pelas suas propriedades anti-convulsivas, que aparentam ser uma consequência da sua elevada afinidade com o receptor CB1, comportando-se como um agonista (que provoca uma acção) parcial do mesmo. [16]
O CDB (canabidiol), componente activo da planta canábis, destacou-se nos últimos anos com vários estudos científicos que comprovaram o seu potencial terapêutico no controlo de vários tipos de Epilepsia. [17] [18]
Embora o modo de acção exacto deste fitocanabinóide seja ainda desconhecido, pressupõe-se que o efeito na excitabilidade neuronal resulte da sua habilidade de activar receptores como o vanilóide e, desta forma, influenciar a libertação e recaptação de importantes neurotransmissores como o glutamato e a adenosina [19][20][21].
As propriedades anti-convulsivantes, aliadas à reduzida toxicidade para o organismo, [22] tornaram o CBD uma ferramenta valiosa no controlo de crises epilépticas refractárias a outros medicamentos. [23][24]
Vários estudos comprovam também as propriedades neuro-protectoras do CBD, reduzindo a hiperexcitabilidade neuronal [25], preservando desta forma as capacidades cognitivas e reduzindo a progressão dos danos causados no sistema nervoso devido a convulsões repetidas. Estas propriedades conferem ao CBD uma boa capacidade neuro protectora [26][27], sem taxa de toxicidade ou perigo de sobredosagem, associada ao uso prolongado de medicamentos anti-epilépticos convencionais [28][29].
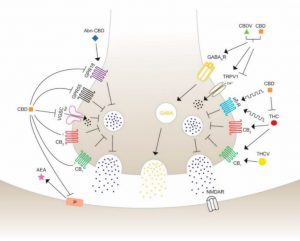
Senn, L., Cannazza, G., & Biagini, G. (2020). Receptors and channels possibly mediating the effects of phytocannabinoids on seizures and epilepsy
Em 2013 foi realizado um questionário a pais de crianças com epilepsia refractária sob tratamento à base de canabinóides. Os participantes relataram 85% de redução do número de convulsões, 14% sem convulsões durante o período de tratamento, 9% não observou qualquer alteração a nível da frequência das convulsões e 4% relatou um aumento das mesmas.
Apesar da prevalência de efeitos adversos ter diminuído ao longo do tratamento com as preparações de canábis, os efeitos secundários mais frequentemente relatados foram sonolência (12,8%), fadiga (9,4%), irritabilidade (9,4%) e náuseas (6,8%). Os entrevistados relataram melhoria no padrão de sono (53%), estado de alerta (71%) e humor (63%). [33]
Em 2015, um estudo realizado com extracto de canábis administrado por via oral demonstrou a melhoria dos sintomas de Epilepsia refractária em doentes pediátricos. [30] Neste mesmo ano, foi realizado um questionário a pais de crianças com Epilepsia refractária que recorreram a um tratamento à base de canabinóides. Cerca de 42% dos pais relatou uma redução superior a 80% na frequência de convulsões, 16% observou uma redução superior a 50% na frequência de convulsões, 16% relatou uma redução superior a 25%, e 16% não teve nenhuma redução. Além disso, 60% dos pais referiu uma diminuição da administração de outros anti-epilépticos após início de tratamento com CBD. Os efeitos positivos incluíram também a melhoria do estado humor (79%), melhoria nos níveis de concentração (74%) e melhoria no padrão de sono (68%). Os efeitos adversos relatados incluíram fadiga (16%) e sonolência (37%). [32]
Recentemente, um estudo que envolveu 214 doentes (com idade entre 1 e 30 anos) com Epilepsia severa, intratável, com início na infância e resistente ao tratamento, revelou uma redução da frequência das convulsões após início de tratamento à base de canabinóides. [31]
A GW Pharmaceuticals lançou quatro ensaios clínicos randomizados para a avaliação da solução oral de CBD (Epidiolex) em Epilepsia pediátrica resistente aos tratamentos convencionais, nomeadamente na síndrome de Dravet (DS) e Lennox-Gastaut (LGS). O estudo da GW Pharmaceuticals randomizou 225 doentes, com uma idade média de 16 anos. Os doentes que tomaram Epidiolex obtiveram uma redução nas crises de 37% ou 42% com 10 ou 20 mg/kg/dia, respectivamente, em comparação com 17% no placebo. Embora, em geral, tenha sido bem tolerado, 26 doentes no tratamento com Epidiolex e oito com placebo relataram um efeito adverso grave.
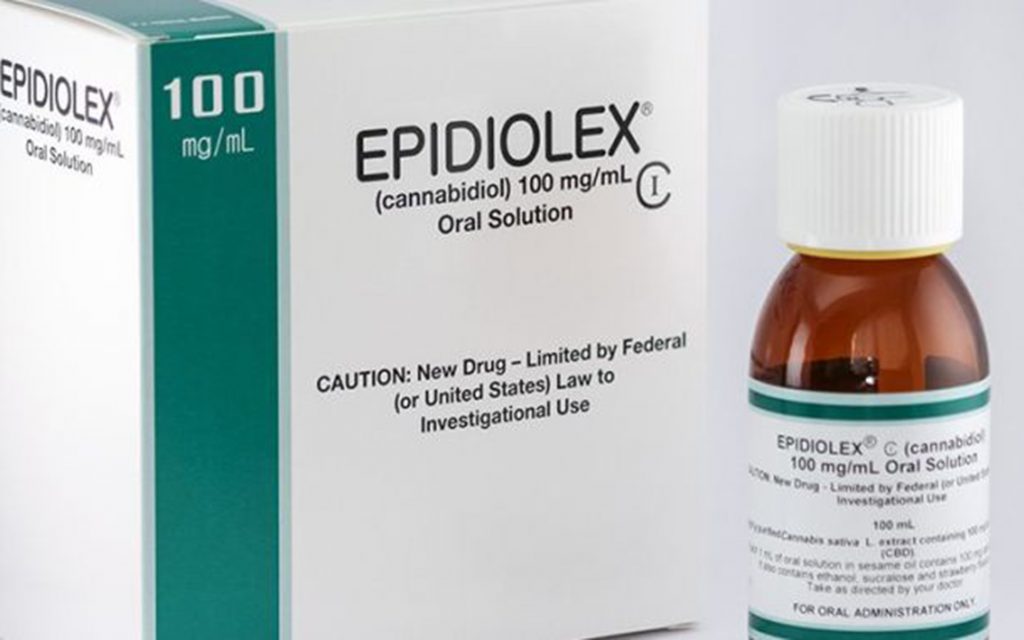
O Epidiolex, da GW Pharma, ainda não foi aprovado pela Agência Europeia do Medicamento (EMA)
Estes resultados permitiram a aprovação, em 2018, do Epidiolex pela FDA para a síndrome de Dravet e Lennox-Gastaut, constituindo uma alternativa para estes doentes, particularmente, na Epilepsia refractária aos tratamentos convencionais. Até ao momento, o Epidiolex não foi aprovado pela EMA.
Em Portugal, a Lei n.º 33/2018, de 18 de Julho, que estabelece o quadro legal para a utilização de medicamentos, preparações e substâncias à base da planta da canábis para fins medicinais, nomeadamente a sua prescrição e dispensa em farmácia, aprovou a canábis como tratamento da Epilepsia e tratamento de transtornos convulsivos graves na infância, tais como as síndromes de Dravet e Lennox-Gastaut.
Canabinóides isolados vs Extractos de Canábis
Os benefícios da utilização de fitocanabinóides isolados é um tema que ainda gera alguma controvérsia na comunidade médica e científica. [34] Existem relatos de inúmeros pacientes que enaltecem os benefícios da utilização da planta completa em relação aos extractos isolados de componentes da mesma. Observa-se maior eficácia no tratamento com recurso a menos quantidade e efeitos adversos.
Estudos realizados em humanos sugerem o potencial do CBD na atenuação dos efeitos do THC, nomeadamente a nível da cognição/memória. [35][36][37]
Um estudo recente relatou que é necessária uma dose 4 vezes menor de extracto de cânhamo para alcançar os mesmos efeitos terapêuticos quando comparado com a utilização de extracto de CBD isolado. [38] Além disso, o mesmo estudo concluiu que existe uma menor incidência de efeitos adversos quando utilizado o extracto de cânhamo.
Os benefícios decorrentes da utilização de um extracto completo da planta vs isolado sustentam a hipótese sugerida por Ethan Russo, conhecido Neurologista e Farmacologista, de que o verdadeiro potencial desta planta reside na combinação sinérgica entre os vários componentes, o chamado “efeito Entourage”. [34]
Bibliografia
- Pertwee RG. Endocannabinoids and Their Pharmacological Actions. Handb Exp Pharmacol 231: 1‐37, 2015.
- Maccarrone M, Valensise H, Bari M, Lazzarin N, Romanini C, and Finazzi‐Agrò A. Progesterone up‐regulates anandamide hydrolase in human lymphocytes: role of cytokines and implications for J Immunol 166: 7183‐7189, 2001.
- Wolfson ML, Muzzio DO, Ehrhardt J, Franchi AM, Zygmunt M, and Jensen F. Expression analysis of cannabinoid receptors 1 and 2 in B cells during pregnancy and their role on cytokine production. J Reprod Immunol 116: 23‐27, 2016.
- Piomelli D, Giuffrida A, Calignano A, and Rodríguez de Fonseca F. The endocannabinoid system as a target for therapeutic drugs. Trends Pharmacol Sci 21: 218‐224, 2000.
- Pertwee RG, ed. Endocanabinóides. In: The Handbook of Experimental Pharmacology. Vol 231. Suíça: Springer International Publishing; 2015
- Lu Y, Anderson HD. Cannabinoid signaling in health and disease. Can J Physiol Pharmacol. 2017;95(4):311-327.
- National Academies of Sciences, Engineering, and Medicine. The Health Effects of Cannabis and Cannabinoids: The Current State of Evidence and Recommendations for Research. Washington, DC: The National Academies Press. 2017; https://www.nap.edu/read/24625/chapter/1. Accessed August 12, 2019.
- . Sugaya Y, Kano M. Control of excessive neural circuit excitability and prevention of epileptic seizures by endocannabinoid signalling. Cell Mol Life Sci 2018;75:2793–2811.
- Camilleri M. Cannabinoids Lu Y, Anderson HD. Cannabinoid signaling in health and disease. Can J Physiol Pharmacol. 2017;95(4):311-327.
- Liu B, Song S, Jones PM, Persaud SJ. GPR55: from orphan to metabolic regulator? Pharmacol Ther. 2015;145:35-42.
- Hanus LO, Meyer SM, Mu~noz E, Taglialatela-Scafati O, Appendino G. Phytocannabinoids: a unified critical inventory. Nat Prod Rep 2016;33:1357–1392.
- Adams R, Pease DC, Clark JH. Isolation of cannabinol, cannabidiol and quebrachitol from red oil of Minnesota wild Hemp. J Am Chem Soc 1940;62:2194–2196.
- Wollner HJ, Matchett JR, Levine J, Loewe S. Isolation of a physiologically active tetrahydrocannabinol from cannabis Sativa resin. J Am Chem Soc 1942;64:26–29.
- Mechoulam R, Shvo Y. Hashish. The structure of cannabidiol. Tetrahedron 1963;19:2073–2078.
- Gaoni Y, Mechoulam R. Isolation, structure, and partial synthesis of an active constituent of Hashish. J Am Chem Soc 1964;86:1646–1647.
- Ameri A, Wilhelm A, Simmet T. Effects of endogenous cannabinoid, anandamide, on neuronal activity in rat hippocampal slices. Br J Pharmacol 1999;126:
- Devinsky O and other. Cannabidiol in patients with treatment-resistant epilepsy: an open-label interventional trial. Lancet Neurol. 2016 Mar;15(3):270-8.
- Devinsky O and other. Cannabidiol: pharmacology and potential therapeutic role in epilepsy and other neuropsychiatric disorders. 2014 Jun;55(6):791-802
- De Petrocellis L, Ligresti A, Moriello AS, Allara M, Bisogno T, Petrosino S, et al. Effects of cannabinoids and cannabinoid-enriched Cannabis extracts on TRP channels and endocannabinoid metabolic enzymes. Br J Pharmacol. 2011;163:1479-94. doi: 10.1111/j.1476-5381.2010.01166.x.
- Campos AC, Ferreira FR, Guimarães FS. Cannabidiol blocks long-lasting behavioral consequences of predator threat stress: possible involvement of 5HT1A receptors. J Psychiatr Res. 2012;46:1501-10. doi: 10.1016/j.jpsychires.2012.08.012.
- Sylantyev S, Jensen TP, Ross RA, Rusakov DA. Cannabinoid- and lysophosphatidylinositol-sensitive receptor GPR55 boosts neurotransmitter release at central synapses. Proc Natl Acad Sci U S A. 2013;110:5193-8. doi: 10.1073/pnas.1211204110.
- Bergamaschi MM, Queiroz RH, Zuardi AW, Crippa JA. Safety and side effects of cannabidiol, a Cannabis sativa constituent. Curr Drug Saf. 2011 Sep 1;6(4):237-49.
- Fabio Arturo Iannotti and other. Nonpsychotropic Plant Cannabinoids, Cannabidivarin (CBDV) and Cannabidiol (CBD), Activate and Desensitize Transient Receptor Potential Vanilloid 1 (TRPV1) Channels in Vitro: Potential for the Treatment of Neuronal Hyperexcitability. ACS Chem. Neurosci., 2014, 5 (11), pp 1131–1141
- Fabio Arturo Iannotti and other. Nonpsychotropic Plant Cannabinoids, Cannabidivarin (CBDV) and Cannabidiol (CBD), Activate and Desensitize Transient Receptor Potential Vanilloid 1 (TRPV1) Channels in Vitro: Potential for the Treatment of Neuronal Hyperexcitability. ACS Chem. Neurosci., 2014, 5 (11), pp 1131–1141
- Hampson AJ, Grimaldi M, Lolic M, Wink D, Rosenthal R, Axelrod J. Neuroprotective antioxidants from marijuana. Ann N Y Acad Sci. 2000;899:274-82.
- Hampson AJ, Grimaldi M, Lolic M, Wink D, Rosenthal R, Axelrod J. Neuroprotective antioxidants from marijuana. Ann N Y Acad Sci. 2000;899:274-82.
- Campos AC, Fogaça MV, Sonego AB, Guimarães FS. Cannabidiol, neuroprotection and neuropsychiatric disorders. Pharmacol Res. 2016 Oct;112:119-127.
- Bergamaschi MM, Queiroz RH, Zuardi AW, Crippa JA. Safety and side effects of cannabidiol, a Cannabis sativa constituent. Curr Drug Saf. 2011 Sep 1;6(4):237-49.
- Gram L, Bentsen KD. Hepatic toxicity of antiepileptic drugs: a review. Acta Neurol Scand Suppl. 1983;97:81-90
- Press CA, Knupp KG, Chapman KE. Parental reporting of response to oral cannabis extracts for treatment of refractory epilepsy. Epilepsy Behav. 2015 Apr;45:49-52.
- Devinsky O, Marsh E, Friedman D, Thiele E, Laux L, Sullivan J, et al. Cannabidiol in patients with treatment-resistant epilepsy: an open-label interventional trial. Lancet Neurol. 2016;15:270-8. doi: 10.1016/S1474-4422(15)00379-8.
- Porter BE, Jacobson C. Report of a parent survey of cannabidiol-enriched cannabis use in pediatric treatment-resistant epilepsy. Epilepsy Behav 2013 Dec;29(3):574-7
- Hussain SA, Zhou R, Jacobson C, Weng J, Cheng E, Lay J, Hung P, Lerner JT, Sankar R. Perceived efficacy of cannabidiol-enriched cannabis extracts for treatment of pediatric epilepsy: A potential role for infantile spasms and lennox-gastaut syndrome. Epilepsy Behav 2015 Jun;47:138-41.
- Russo, E.B. Taming THC: Potential cannabis synergy and phytocannabinoid-terpenoid entourage effects. Br. J. Pharmacol. 2011, 163, 1344–1364.
- Morgan, C.J.; Schafer, G.; Freeman, T.P.; Curran, H.V. Impact of cannabidiol on the acute memory and psychotomimetic effects of smoked cannabis: Naturalistic study: Naturalistic study [corrected]. Br. J. Psychiatry. 2010, 4, 285–290. [CrossRef]
- Hayakawa, K.; Mishima, K.; Hazekawa, M.; Sano, K.; Irie, K.; Orito, K.; Egawa, T.; Kitamura, Y.; Uchida, N.; Nishimura, R.; et al. Cannabidiol potentiates pharmacological effects of ∆9-tetrahydrocannabinol via CB1 receptor-dependent mechanism. Brain Res. 2008, 1188, 157–164.
- Osborne, A.L.; Solowij, N.; Weston-Green, K. A systematic review of the effect of cannabidiol on cognitive function: Relevance to schizophrenia. Neurosci. Biobehav. Rev. 2017, 72, 310–324.
- Pamplona, F.A.; Rolim da Silva, L.; Coan, A.C. Potential Clinical Benefits of CBD-Rich Cannabis Extracts Over Purified CBD in Treatment-Resistant Epilepsy: Observational Data Meta-analysis. Front. Neurol. 2018, 9, 759.
*Soraia Tomás é Enfermeira, licenciada pela Escola Superior de Enfermagem de Coimbra em 2015. Desempenhou funções nos cuidados intensivos de cirurgia Cardio-Torácica e transplantação pulmonar em Lisboa. Neste momento trabalha no Spine Center, serviço de cirurgia à coluna e unidade de cuidados intensivos de cirurgia geral no Hospital da Luz em Coimbra, cidade onde reside. Entusiasta na área da Canábis Medicinal, é membro do conselho científico do Observatório Português de Canábis Medicinal, esteve presente em conferências neste âmbito (Portugal Medical Cannabis, Cannabis Europa, CannX, entre outras) e obteve uma pós-graduação em GMP’s para Canábis Medicinal, curso realizado pelo Observatório Português de Canábis Medicinal em parceria com o Laboratório Militar de Produtos Químicos e Farmacêuticos e a Faculdade de Farmácia da Universidade de Lisboa. Presidente da Direcção da APCANNA – Associação Portuguesa de Informação sobre Canábis, pretende desenvolver projetos dedicados à divulgação, educação e formação em canábis medicinal a profissionais de saúde e ao público em geral, promovendo desta forma a excelência na prática profissional e o acesso seguro e eficaz a terapias com canabinóides.
____________________________________________________________________________________________________
[Aviso: Por favor, tenha em atenção que este texto foi originalmente escrito em Português e é traduzido para inglês e outros idiomas através de um tradutor automático. Algumas palavras podem diferir do original e podem verificar-se gralhas ou erros noutras línguas.]____________________________________________________________________________________________________

O que fazes com 3€ por mês? Torna-te um dos nossos Patronos! Se acreditas que o Jornalismo independente sobre canábis é necessário, subscreve um dos níveis da nossa conta no Patreon e terás acesso a brindes únicos e conteúdos exclusivos. Se formos muitos, com pouco fazemos a diferença!
Notícias Relacionadas
-


Snoop Dogg e o seu “next episode” na indústria canábica europeia
-


Tailândia declara quatro variedades de canábis como património nacional
-


Fluence anuncia presença e lançamento de novos produtos na GreenTech Amsterdam 2023
-


Portugal: SOMAÍ recebe certificação EU-GMP e obtém €5 milhões de financiamento
-


Itália: Supremo Tribunal decide que cultivo de canábis para consumo próprio não é crime
-
Reino Unido avança com ensaios clínicos com Sativex em pacientes com tumores cerebrais

Mais recentes


O 4:20 está a chegar e há celebrações no Porto e em Lisboa
A data da celebração da cultura da canábis está a chegar! Este sábado, 20 de Abril, é o dia em...


Paul Bergholts, alegado líder da Juicy Fields, detido na República Dominicana
Paul Bergholts, o alegado líder do esquema em pirâmide Juicy Fields, terá sido detido na República Dominicana e será submetido a...


Canabinóides revelam resultados promissores no tratamento do Transtorno da Personalidade Borderline
Uma investigação levada a cabo pela Khiron LifeSciences e coordenada por Guillermo Moreno Sanz sugere que os medicamentos à base de...


Caso Juicy Fields: 9 detidos pela Europol e Eurojustice. Burla ultrapassa 645 milhões de euros
Uma investigação conjunta conduzida por várias autoridades europeias, apoiadas pela Europol e pela Eurojust, culminou na detenção de nove suspeitos...


Utilizadores regulares de canábis podem necessitar de mais anestesia durante procedimentos médicos
Os utilizadores regulares de canábis podem necessitar de mais anestesia durante os procedimentos médicos para permanecerem sedados, se comparados com...


O futuro do CBD no Japão: Como as reformas legais irão moldar o mercado
No final do ano passado, o Japão deu um grande passo em direcção à reforma da canábis depois de aprovar...


Portugal: GreenBe Pharma obtém certificação EuGMP nas instalações de Elvas
A GreenBe Pharma, uma empresa de canábis medicinal localizada em Elvas, Portugal, obteve a certificação EU-GMP, ao abrigo dos regulamentos...


Álvaro Covões, da Everything is New, compra instalações da Clever Leaves no Alentejo por 1.4 milhões de euros
Álvaro Covões, fundador e CEO da agência promotora de espectáculos ‘Everything is New‘, que organiza um dos maiores festivais de...


ICBC regressa a Berlin a 16 e 17 de Abril
É uma das maiores e mais reconhecidas conferências de B2B sobre canábis da Europa e regressa a Berlim já nos...


A legalização da canábis na Alemanha vista pelos olhos do hacker que criou um mapa essencial
Um hacker de Koblenz, uma cidade do estado da Renânia-Palatinado, criou um mapa com os locais onde, a partir de...







