L'autisme est une affection neurologique développementale présente dès l'enfance et permanente, qui se caractérise généralement par des difficultés de communication et d'interaction sociale. Le terme trouble du spectre autistique (TSA) est utilisé pour définir un ensemble de troubles neuropsychiatriques du développement de l'enfant, résultant de dysfonctionnements dans le développement du système nerveux central. Il existe cinq types de troubles, mais les principaux sont l'autisme classique, le syndrome d'Asperger et le trouble du développement non spécifié. [1]
Troubles du spectre autistique
Selon l'American Psychiatric Association, le trouble du spectre autistique est "un syndrome neurocomportemental résultant de troubles du système nerveux central qui affectent le développement typique de l'enfant. Les symptômes apparaissent au cours des trois premières années de la vie et comprennent trois grands domaines de perturbation : social, comportemental et communicationnel » [2]
Il n'y a toujours pas de cause définie pour l'autisme et le traitement pharmacologique actuel offre une efficacité limitée et des effets secondaires graves qui compromettent son adhésion.
L'influence du système endocannabinoïde sur les troubles du spectre autistique
Au cours de la dernière décennie, plusieurs études précliniques et cliniques ont été structurées afin d'analyser les changements liés à la modulation du système endocannabinoïde et à l'administration de cannabinoïdes chez les patients atteints d'autisme ou de troubles généralisés du développement.
De ces études, il a été possible de conclure que :
- La plupart des médicaments approuvés pour le contrôle des symptômes associés aux TSA ont une faible efficacité et un risque élevé d'effets indésirables. Une revue de la littérature publiée en 2022 a évalué l'efficacité de nouveaux agents pharmacologiques à cet effet. La plupart des essais cliniques randomisés réalisés (avec la fluoxétine et l'ocytocine, par exemple) ont eu des résultats négatifs ou non concluants. Deux études multicentriques avec la bumétadine ont été interrompues prématurément faute d'efficacité, le seul essai clinique ayant montré des résultats prometteurs pour les comportements perturbateurs ayant été mené avec des médicaments à base de cannabinoïdes. [3]
- Les altérations associées au PEA sont étroitement liées à un état inflammatoire généralisé du système nerveux central et immunitaire [4] ainsi qu'à des altérations majeur au niveau intestinal [5,6] et les différents composants du système endocannabinoïde sont présents à des concentrations élevées dans le système nerveux et le tractus gastro-intestinal.
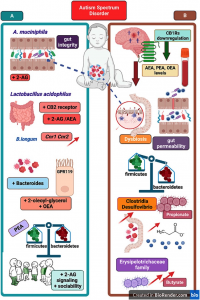
"Le partenariat endocannabinoïdes-microbiote dans l'homéostasie de l'axe intestin-cerveau : implications pour les troubles du spectre autistique"
- L'administration de médicaments à base de cannabinoïdes a principalement permis de réduire de multiples symptômes, tels que l'automutilation, l'hyperactivité ou les troubles du sommeil, par exemple, améliorant ainsi la qualité de vie du patient et de ses soignants. Les mêmes études révèlent que le traitement aux cannabinoïdes est une option bien tolérée, sûre et efficace pour soulager les symptômes associés aux modifications du spectre autistique [7-9]
Sur la base des essais cliniques randomisés en double aveugle menés à ce jour sur ce sujet, nous savons que :
- En 2021, Adi Aran et son équipe ont administré un extrait de chémotype III (CBD : THC – 20:1) à des enfants atteints de TSA aux comportements perturbateurs. En plus d'être bien toléré, le traitement aux cannabinoïdes a démontré une réduction significative de 49 % de ce type de comportement par rapport au groupe placebo. [dix]
- Le striatum (noyau caudé, Putamen et noyau Accumbens) joue un rôle crucial au cours du développement et sa connectivité fonctionnelle atypique (FC) peut contribuer au développement de multiples symptômes associés aux TSA. En 2021, Pretzsch C. et al ont démontré que l'administration de CBDV (cannabidivarine, 600 mg) modulait la FC atypique des individus atteints de TSA vers leur fonction neuro typique [11]. En 2019, le même auteur a rapporté des changements liés à l'administration de cannabidiol (CBD) dans la modulation des métabolites (GABA et glutamate) et la régulation de l'amplitude fonctionnelle des fluctuations à basse fréquence (fALFF) et du CF entre les régions systématiquement impliquées dans le PEA [12,13, XNUMX].
- En 2020, au Brésil, Estácio Amaro da Silva Júnior et ses collègues ont conclu que l'administration d'un extrait de chémotype III améliorait les niveaux d'anxiété, d'agitation psychomotrice, d'interaction sociale et de capacité de concentration chez 30 enfants atteints de TSA par rapport au groupe placebo. [14]
- En 2018, en Iran, Mona Khalaj et ses collègues ont suggéré que l'administration de l'endocannabinoïde palmitoyléthanolamide pourrait agir en synergie avec la rispéridone pour atténuer les niveaux d'hyperactivité et d'irritabilité associés à l'autisme, grâce à sa capacité à réduire l'inflammation et l'hyperstimulation du système glutamatergique. . [15]
Enfin, il est également important de mentionner qu'en 2021, la première étude observationnelle a été développée, qui visait à déterminer le potentiel de la pharmacométabolomique dans l'identification de biomarqueurs métaboliques qui répondent au traitement aux cannabinoïdes. Des enquêtes comportementales ont été appliquées avant le prélèvement de 2 échantillons de salive (avant et environ 90 à 120 minutes après l'administration de médicaments à base de cannabinoïdes) à 9 enfants sains et 15 enfants autistes (sans antécédent d'épilepsie) sous traitement aux cannabinoïdes (THC - 0.05 à 50 mg et CBD – 7.5 à 200 mg).
Par la suite, des modifications de plusieurs biomarqueurs (N-acétyl-aspartate (NAA), spermine, cortisol, sulfate de déhydroépiandrostérone et glutamine, entre autres) ont été évaluées, qui, selon les auteurs, après l'administration de la dose matinale de médicaments à base de cannabinoïdes , ont atteint des niveaux physiologiques identiques à ceux des enfants au développement typique.
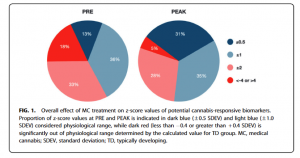
"Le potentiel des biomarqueurs sensibles au cannabis à base de lipides salivaires pour évaluer le traitement du cannabis médical chez les enfants atteints de troubles du spectre autistique."
Publié dans la revue Recherche sur le cannabis et les cannabinoïdes et menée par le Dr Bonni Goldstein, pédiatre de Los Angeles, avec plus de 13 ans de pratique clinique avec les cannabinoïdes, cette étude a permis d'identifier le profil métabolique des enfants atteints de TSA avec une réponse thérapeutique positive au traitement aux cannabinoïdes. On peut donc considérer les biomarqueurs Cannabis-Responsive™ comme une mesure universelle d'analyse de l'impact physiologique du traitement aux cannabinoïdes, qui fournit aux professionnels de santé des données objectives et quantitatives, leur permettant de personnaliser et d'optimiser le traitement aux cannabinoïdes en tenant compte du profil de chaque individu. [16,17]
BIBLIOGRAPHIE
Fédération portugaise de l'autisme – Consulté le 28 juillet 2022 sur : https://www.fpda.pt/
[2] Association américaine de psychiatrie (2013). Trouble du spectre de l'autisme - Dans Manuel diagnostique et statistique des troubles mentaux (5e éd.)
[3] Baribeau, D., Vorstman, J. & Anagnostou, E. Nouveaux traitements dans les troubles du spectre autistique. Curr. Opin. Psychiatrie 35, 101-110 (2022). Doi : 10.1097/YCO.0000000000000775
[4] Siniscalco, D., Schultz, S., Brigida, A. et Antonucci, N. Inflammation et dysrégulations neuro-immunes dans les troubles du spectre autistique.Pharmaceutiques 11, 56. (2018). https://doi.org/10.3390/ph11020056
[5] McElhanon, BO, McCracken, C., Karpen, S. et Sharp, WG Symptômes gastro-intestinaux dans les troubles du spectre autistique : une méta-analyse. Pédiatrie 133 (5), 872–883.(2014). doi : 10.1542/peds.2013-3995
[6] Coccurello R, Marrone MC et Maccarrone M. Le partenariat endocannabinoïdes-microbiote dans l'homéostasie de l'axe intestin-cerveau : implications pour les troubles du spectre autistique. De face Pharmacol. 13:869606. (2022) doi : 10.3389/ffhar.2022.869606
[7] Aran A, Cassuto H, Lubotzky A et al. Bref rapport : Le cannabis riche en cannabidiol chez les enfants atteints de troubles du spectre autistique et de graves problèmes de comportement – Une étude de faisabilité rétrospective. J Autism Dev Disord 49: 1284–1288. (2018) doi:10.1007/s10803-018-3808-2
[8] Bar-Lev Schleider, L., Mechoulam, R., Saban, N., Meiri, G. et Novack, V. Real Life Expérience du traitement du cannabis médical dans l'autisme : analyse de l'innocuité et de l'efficacité. Sci. représentant 9, 200. (2019). doi:10.1038/S41598-018-37570-Y
[9] Fleury-Teixeira, P., Caixeta, FV, Ramires da Silva, LC et Brasil-Neto, R. Effets de l'extrait de Cannabis Sativa enrichi en CBD sur les symptômes des troubles du spectre autistique : une étude observationnelle de 18 participants subissant une utilisation compassionnelle. De face. Neurol. 10. (2019). doi : 10.3389/fneur.2019.01145
[10] Aran et al. Traitement cannabinoïde pour l'autisme : un essai randomisé de preuve de concept. Mol. autisme (2021) 12: 6. https://doi.org/10.1186/s13229-021-00420-2
[11] Pretzsch, Charlotte M., Floris, Dorothea L., Voinescu, Bogdan, Elsahib, Malka, Mendez, Maria A., Wichers, Robert, Ajram, Laura et al., Modulation des différences de connectivité fonctionnelle striatale chez les adultes avec et sans trouble du spectre autistique dans un essai randomisé à dose unique de cannabidivarine. Mol. autisme 12 (1). (2021) https://doi.org/10.1186/s13229-021-00454-6.
[12] Pretzsch CM, Voinescu B, Mendez MA, Wichers R, Ajram L, Ivin G et al. L'effet du cannabidiol (CBD) sur l'activité à basse fréquence et la connectivité fonctionnelle dans le cerveau des adultes avec et sans trouble du spectre autistique (TSA). J Psychopharmacol. 2019;33:1141–8. (2019) https://doi.org/10.1177/0269881119858306
[13] Pretzsch CM, Freyberg J, Voinescu B, Lythgoe D, Horder J, Mendez MA et al. Effets du cannabidiol sur les systèmes d'excitation et d'inhibition du cerveau ; un essai randomisé à dose unique contrôlé par placebo pendant la spectroscopie par résonance magnétique chez des adultes avec et sans trouble du spectre autistique. Neuropsychopharmacology.;44(8):1398–405. (2019); https://doi.org/10.1038/s41386-019-0333-8
[14] Junior E. et coll. Évaluation de l'efficacité et de l'innocuité de l'extrait de cannabis riche en cannabidiol chez les enfants atteints de troubles du spectre autistique : essai clinique randomisé, en double aveugle et contrôlé contre placebo. Trends Psychiatry Psychother - Article de journal pré-preuve (2020) http://dx.doi.org/10.47626/2237-6089-2021-0396
[15] Khalaj M, Saghazadeh A, Shirazi E, Shalbafan MR, Alavi K, Shooshtari MH, et al. Le palmitoyléthanolamide comme traitement d'appoint pour l'autisme : résultats d'efficacité et d'innocuité d'un essai contrôlé randomisé. J. Psychiatr. Res. 103, 104-111. (2018) https://doi.org/10.1016/j.jpsychires.2018.04.022
[16] Siani-Rose M., Cox S., Goldstein B., Abrams D., Taylor M., Kurek I Biomarqueurs sensibles au cannabis : une application basée sur la pharmacométabolomique pour évaluer l'impact du traitement au cannabis médical sur les enfants atteints de troubles du spectre autistique. Recherche sur le cannabis et les cannabinoïdes X:X, 1-12, (2021) DOI : 10.1089/can.2021.0129
[16] Siani-Rose M., McKee R., Cox S., Goldstein B., Abrams D., Taylor M., Kurek I. Le potentiel des biomarqueurs sensibles au cannabis à base de lipides salivaires pour évaluer le traitement du cannabis médical chez les enfants atteints de troubles du spectre autistique. Recherche sur le cannabis et les cannabinoïdes X:X, 1-15 (2022) DOI : 10.1089/can.2021.0224.
___________________________________________________________________
* Soraia Tomás est infirmière, diplômée de l'Escola Superior de Enfermagem de Coimbra en 2015. Elle a travaillé dans les soins intensifs de chirurgie cardio-thoracique et de transplantation pulmonaire à Lisbonne. Il travaille actuellement au Spine Center, un service de chirurgie de la colonne vertébrale et une unité de soins intensifs de chirurgie générale à l'hôpital da Luz de Coimbra, la ville où il réside. Enthousiaste dans le domaine du cannabis médicinal, il est membre du conseil scientifique de l'Observatoire portugais du cannabis médicinal, a assisté à des conférences dans ce domaine (Portugal Medical Cannabis, Cannabis Europa, CannX, entre autres) et a obtenu un diplôme de troisième cycle en GMP pour Cannabis Médicinal, cours réalisé par l'Observatoire Portugais du Cannabis Médicinal en partenariat avec le Laboratoire Militaire des Produits Chimiques et Pharmaceutiques et la Faculté de Pharmacie de l'Université de Lisbonne. Président du conseil d'administration de l'APCNNA - Association portugaise pour l'information sur le cannabis, a l'intention de développer des projets dédiés à la diffusion, à l'éducation et à la formation au cannabis médical auprès des professionnels de la santé et du grand public, promouvant ainsi l'excellence dans la pratique professionnelle et un accès sûr et efficace aux cannabinoïdes thérapies.
































