A Tilray только что одобрила свое первое «вещество или препарат на основе каннабиса» в Португалии, получив ACM (разрешение на размещение на рынке) от ИНФАРМЕД, ИП для сухоцветов с содержанием ТГК 18% и КБД менее 1%. Это второй продукт на основе каннабиса, одобренный в Португалии (первым был Sativex), и он увидел свет после более чем года ожидания. Цена пока не утверждена и пока неизвестно, будет ли она возмещена.
Новость была опубликована сегодня утром агентством Agência Lusa и воспроизведена несколькими СМИ, такими как Diário de Notícias, Общественность, наблюдатель, SIC News или Сапо 24, но ни один из них не уточняет, какое вещество одобрено и при каких патологиях оно показано. В пресс-релизе Tilray не упоминается, какой продукт или вещество получило ACM, но информация об одобренном продукте уже доступна на веб-сайте Infarmed.

Завод Tilray в Кантанхеде, округ Коимбра, Португалия.
Источник Infarmed заверил Cannareporter, что цена является обязательным условием доступности продукта по рецепту, и она пока не определена. Более того, Infarmed заявляет, что запросить взнос должна также компания-владелец ACM. Тилрэй подтвердил Cannareporter, что цена еще не утверждена, поэтому пока неизвестно, будет ли она возмещена государством.
В беседе с Cannareporter Рита Барата, директор по маркетингу в Европе и региональный менеджер Tilray на Пиренейском полуострове: заявил, что не может предоставить дополнительную информацию, кроме пресс-релиза, и что цена на этот продукт «ждет»r оценка и одобрение со стороны Infarmed». Что касается доступности новых продуктов на португальском рынке, Рита Барата говорит, что «мы надеемся подать новые запросы ACM в Infarmed в ближайшем будущем».
В чем разница между лекарством и веществом или препаратом на основе каннабиса?
В заявлении Tilray говорится, что это «первый и единственный препарат или вещество на основе растения каннабис для медицинских целей, разрешенное в нашей стране», несмотря на то, что Sativex уже существует в Португалии, разрешен в Португалии в 2012 году и доступен в больницах. по запросу специального разрешения.
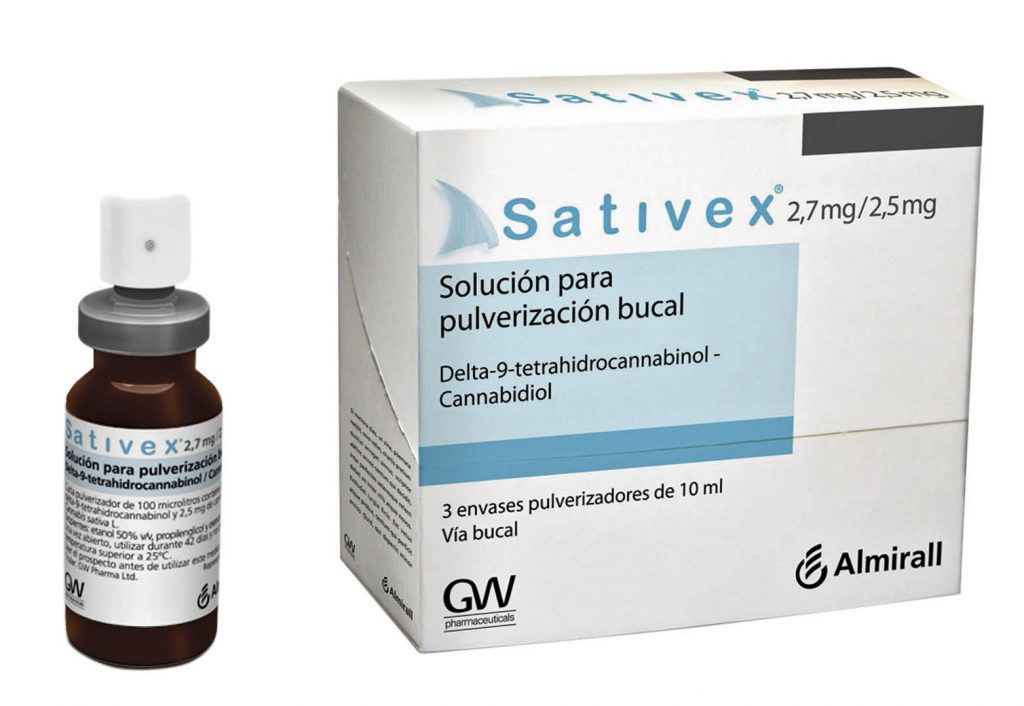
Сативекс, имеющий соотношение ТГК и КБД 1:1, считается лекарством и получил AIM от Infarmed в 2012 году.
Если Infarmed уже одобрило лекарство на основе каннабиса, почему продукт Tilray является «первым и единственным»? Это объясняется тем, что цветы Tilray, одобренные теперь компанией Infarmed, попадают в категорию «веществ и препаратов на основе каннабиса», для которых требуется ACM – регистрационное удостоверение. Источник из Infarmed объяснил Cannareporter, что ACM – это «способ упростить выход лекарственных продуктов из каннабиса на португальский рынок, поскольку AIM – регистрационное удостоверение – приписываемое лекарствам, требует проведения предварительных клинических испытаний для подтверждения их эффективности».
Таким образом, Sativex попадает в категорию «Лекарственные средства», а компания GW Pharmaceuticals, держатель AIM, представляет соответствующие клинические исследования для получения одобрения для Infarmed.
Продукт Tilray, попадающий в категорию «вещества и препараты на основе растения каннабис», фактически является первым и единственным, получившим ACM от Infarmed, так как не требовал клинических испытаний для подтверждения своей эффективности.
Одобрение Infarmed распространяется на цветы каннабиса с содержанием ТГК 18% и КБД менее 1%.
В поиске по сайту информед, от Infarmed теперь можно найти два продукта на основе каннабиса, одобренные Управлением по лекарственным средствам. Сативекс и «Тилрей Флор Сека ТГК 18», цветы с содержанием 18% дельта-9-тетрагидроканнабинола (ТГК) и менее 1% каннабидиола (КБД).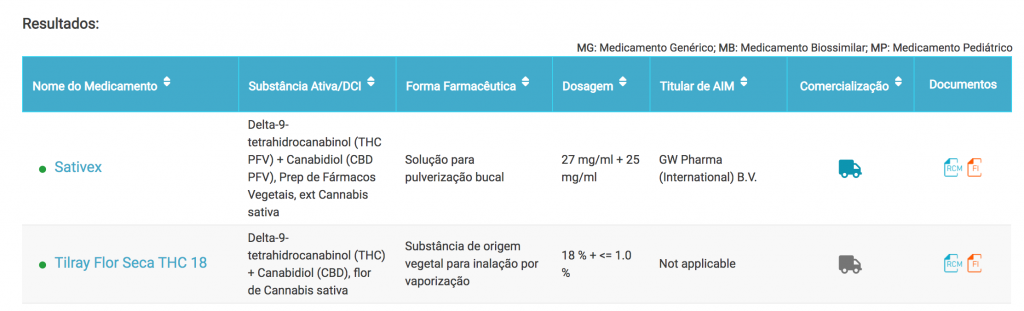
Нет информационный документ для медицинских работников На сайте Инфармед вы можете прочитать, что это лекарство показано только людям в возрасте 25 лет и старше и что его не следует назначать детям или лицам младше 18 лет.
Кроме того, в документе говорится, что «этот продукт показан только в тех случаях, когда традиционные методы лечения не дали ожидаемых эффектов или вызывают соответствующие побочные эффекты. Конкретный состав определяет, как действует каннабис и какие побочные эффекты он может вызвать».
На сайте Инфармед Инструкции по использованию поэтому медицинские работники могут назначать «соцветия с высоким содержанием дельта-9-тетрагидроканнабинола (ТГК >> КБД)» в следующих случаях:
• Тошнота и рвота (в результате химиотерапии, лучевой терапии и комбинированной терапии ВИЧ и лечения гепатита С)
• Стимуляция аппетита при паллиативной помощи пациентам, проходящим онкологическое лечение или больным СПИДом;
• Устойчивая к терапии глаукома. Соцветия с высоким содержанием дельта-9-тетрагидроканнабинола (ТГК) или со сбалансированным содержанием дельта-9-тетрагидроканнабинола и каннабидиола (ТГК >> КБД или ТГК ≈ КБД).
• Хроническая боль (связанная с онкологическими заболеваниями или нервной системой, например, нейропатическая боль, вызванная повреждением нерва, фантомная боль в конечностях, невралгия тройничного нерва или после опоясывающего герпеса)
• Синдром Жиля де ла Туретта
• Спастичность, связанная с рассеянным склерозом или травмами спинного мозга;
O документ также предупреждает, что, учитывая его концентрацию, Tilray Flor Seca THC 18 не показан при эпилепсии и лечении тяжелых судорожных расстройств в детском возрасте, таких как синдромы Драве и Леннокса-Гасто, так как соцветия с высоким содержанием каннабидиола (КБД) и низким дельта- 9-тетрагидроканнабинол (ТГК).
Тилрей рекомендует пользователей, что Flor Seca THC18 «применяется с помощью медицинского испарителя каннабиса, классифицированного как медицинское устройство (например, Volcano Medic или Mighty Medic)», и предупреждает о длинном списке взаимодействий с другими лекарствами и нежелательных эффектах.
Tilray гарантирует, что у нее будет больше продуктов в пути
Tilray также «планирует в ближайшем будущем сделать другие продукты доступными для пациентов в Португалии», сообщила Рита Барата, генеральный директор Tilray, в заявлении, направленном агентству Lusa.
По словам ответственного лица, требования пациентов растут, «и миссия Tilray состоит в том, чтобы предоставлять самые безопасные и качественные продукты, которые максимально отвечают их потребностям».
Производственное подразделение в Кантанхеде имеет все необходимые сертификаты для выращивания и местного производства препаратов и веществ на основе каннабиса для медицинских целей, а также экспорта готовой продукции с сертификатом надлежащей производственной практики по всему Европейскому Союзу и на другие международные рынки, где используется регулируемое растение.
Саша Милкарек, генеральный директор компании в Европе, подчеркивает, что разрешение Infarmed «подтверждает, что медицинские продукты каннабиса Tilray соответствуют самым высоким национальным и международным стандартам».
Tilray — одна из крупнейших компаний в мире, занимающаяся исследованием, выращиванием, производством и распространением медицинского каннабиса. Ее продукция доступна в 16 странах мира. Ее основные мощности находятся в Кантанхеде, округ Коимбра, но компания также занимается выращиванием сельскохозяйственных культур в Эрдаде-ду-Эспоран, в Алентежу, помимо импортировать Большие партии из Уругвая.













































[…] только одна компания (Tilray) получила ACM от Infarmed на производное каннабиса, а именно сушеные цветы с 18% ТГК. Сативекс (от GW […]
[…] только одна компания (Tilray) получила ACM от Infarmed на производное каннабиса, а именно сушеные цветы с 18% ТГК. Сативекс (от GW […]